COVID-19 重症化抑制薬の開発

- 研究代表者
- 渡部 良広
- 所属・役職
- 附属病院 先端医療開発センター 特任教授
- 研究分野
- 創薬科学、先端医療開発、規制科学
- プロジェクトメンバー
- 渡部 良広 (附属病院 先端医療開発センター 特任教授)
材木 義隆 (附属病院 血液内科 医員)
中尾 眞二 (医薬保健研究域 医学系 教授)
研究の概要
新型コロナウイルス(SARS-CoV-2) のパンデミックを克服するため、適応可能な抗ウイルス薬が既存薬リポジショニングや新規開発として進められていますが、SARS-CoV-2感染による症状(COVID-19)重篤化・死亡の原因はウイルス感染に誘導される“サイトカインストーム”とされています。COVID-19重症化患者では、抗ウイルス薬に加えて、“サイトカインストーム”の制御が、急性肺傷害等の臓器機能障害を回避し早期回復を促す上で大変重要と考えられます。
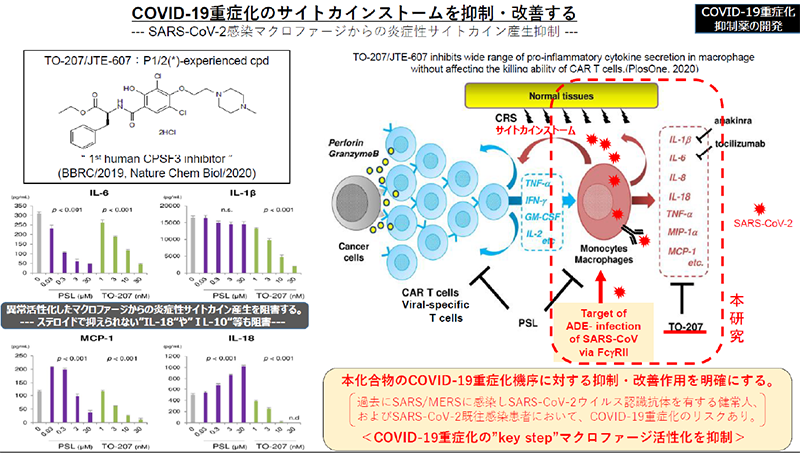
本研究開発においては、このサイトカインストームの発症機序の解明を行い、過去臨床試験にてヒトに投与された経験のある治験薬を用いて治療効果を検討します。即ち、COVID-19重症化のサイトカインストームが抗体依存性感染増強(ADE)を一つの機序として起こること、さらに過去治験薬(JTE-607/TO-207;図参照)によってサイトカインストームが抑制されるかを検討します。研究代表者らは、このJTE-607の作用特徴を、CAR-T療法に併発する“サイトカイン遊離症候群”を抑制することなどにより、明らかにしてきました(PlosOne, 2020)。図左に示すようにJTE-607は、CPSF3 を阻害することにより誘導型炎症性サイトカインのmRNA 成熟を特異的に妨げ、単球・マクロファージからの炎症性サイトカイン産生を強く抑制します。ステロイド(prednisolone; PSL)では抑制されないIL-18 やIL-10 も減少させ、COVID-19 重症化のバイオマーカーであるMCP-1 やIL-8 産生をnM オーダーで強力に阻害する一方で、キラーT細胞(CAR-T細胞やウイルス感染細胞キラーT細胞)に対しては、ステロイド作用と異なり、抑制作用が無いか限定的です。この特徴は、COVID-19のサイトカインストームの回避・抑制効果と、SARS-CoV-2ウイルス排除能の維持に繋がることを強く示唆しています。実際に、遺伝子導入キラーT細胞のCAR-T 細胞療法に伴う“サイトカイン遊離症候群”が、重症COVID-19患者例に見られる“サイトカインストーム”に類似していると報告されました(Science, 2020)。
そこで本研究(図右:赤点線枠)では、この過去治験薬をCOVID-19 重症化改善に適応するためにCOVID-19 重症化機序として想定される「ADE 機序で感染したマクロファージの活性化(サイトカイン産生)」に対して、JTE-607作用が検出されるか、またその作用は臨床上明確な効果を発揮するかについて解析します。
想定される研究成果
本過去治験薬JTE-607/TO-207 に関して、ADE機序によるCOVID-19 重症化抑制作用の強弱およびステロイド等の既存薬に対する優位性が明らかにされます。
COVID-19 重症化のサイトカインストームは、ウイルス特異的キラーT細胞活性化を介した臓器局在(肺など)マクロファージの異常活性化によって惹起されると報告されています(図右:キラーT細胞とMφの関係図を参照)。キラーT細胞との相互作用によるマクロファージ活性化がJTE-607によって阻害されることは、申請者らの最近の報告(CAR-T 細胞によるMφ活性化の阻害作用;PlosOne, 2020)から容易に想定されます。
以上、COVID-19 重症化のサイトカインストームを、上記したADE 機序およびキラーT細胞誘発機序のどちらのマクロファージ異常活性化機序においても、本過去治験薬は重症化を抑制でき、重症例を改善できる可能性が明確となります。